乙炔合成方法
1.电石法:由电石(碳化钙)与水作用得到乙炔。
2.天然气制乙炔法:预热到600~650℃的原料天然气和氧进入多管式烧嘴板乙炔炉,在1500℃下,甲烷裂解制得8%左右的稀乙炔,再用犖甲基吡咯烷酮提浓制得99%的乙炔成品。
乙炔造价信息
乙炔(acetylene)最简单的炔烃,又称电石气。结构式H-C≡C-H,结构简式CH≡CH,最简式(又称实验式)CH,分子式 C2H2,乙炔中心C原子采用sp杂化。电子式 H:C┇┇C:H乙炔分子量 26.4 ,气体比重 0.91(kg/m3),火焰温度3150 ℃,热值12800(kcal/m3)在氧气中燃烧速度 7.5 ,纯乙炔在空气中燃烧2100度左右,在氧气中燃烧可达3600度。化学性质很活泼,能起加成、氧化、聚合及金属取代等反应。
氧化反应
a.可燃性:
b.被KMnO4氧化:能使紫色酸性高锰酸钾溶液褪色。
C₂H₂ 2KMnO₄ 3H₂SO₄=2CO₂ K₂SO₄ 2MnSO₄ 4H₂O
加成反应
可以跟Br₂、H₂、HX等多种物质发生加成反应。如:
与Br₂的加成:
现象:溴水褪色或Br₂的CCl₄溶液褪色
所以可用酸性KMnO₄溶液或溴水区别炔烃与烷烃。
与H2的加成:
与HX的加成:
氯乙烯用于制聚氯乙烯
“聚合”反应
三个乙炔分子结合成一个苯分子:
由于乙炔与乙烯都是不饱和烃,所以化学性质基本相似。在适宜条件下,三分子乙炔能聚合成一分子苯。但苯的产量不高,副产物又多。如果利用钯等过渡金属的化合物作催化剂,乙炔和其他炔烃可以顺利地生成苯及其衍生物。
在一定条件下,乙炔也能与烯烃一样,聚合成高聚物——聚乙炔。
在Ni(CN)2,80~120℃,1.5MPa条件下,4分子乙炔聚合主要生成环辛四烯。
金属取代反应(可用于乙炔的定性鉴定)
将乙炔通入溶有金属钠的液氨里有氢气放出。乙炔与银氨溶液反应,产生白色乙炔银沉淀。
乙炔具有弱酸性,因为乙炔分子里碳氢键是以SP-S重叠而成的。碳氢里碳原子对电子的吸引力比较大些,使得碳氢之间的电子云密度近碳的一边大得多,而使碳氢键产生极性,给出H 而表现出一定的酸性。(pKa=25)
将其通入硝酸银或氯化亚铜氨水溶液,立即生成白色乙炔银(AgC≡CAg)和棕红色乙炔亚铜(CuC≡CCu)沉淀,可用于乙炔的定性鉴定。这两种金属炔化物干燥时,受热或受到撞击容易发生爆炸,如反应完应用盐酸或硝酸处理,使之分解,以免发生危险。注意:乙炔在使用贮运中要避免与铜接触。
酸碱反应
炔烃中C≡C的C是sp杂化,使得Csp-H的σ键的电子云更靠近碳原子,增强了C-H键极性使氢原子容易解离,显示“酸性”。连接在C≡C碳原子上的氢原子相当活泼,易被金属取代,生成炔烃金属衍生物叫做炔化物。
CH≡CH Na → CH≡CNa 1/2H2(条件液氨)
CH≡CH 2Na → CNa≡CNa H2 (条件液氨,190℃~220℃)
CH≡CH NaNH2 → CH≡CNa NH3
CH≡CH Cu2Cl2 (2AgCl) 2NH4OH → CCu≡CCu(CAg≡CAg)↓ 2NH4Cl 2H2O(注意:只有在三键上含有氢原子时才会发生,用于鉴定端基炔RH≡CH)。
其他化学特性
乙炔与铜、银、水银等金属或其盐类长期接触时,会生成乙炔铜(Cu2C2)和乙炔银(Ag2C2)等爆炸性混合物,当受到摩擦、冲击时会发生爆炸。因此,凡供乙炔使用的器材都不能用银和含铜量70%以上的铜合金制造。
储存注意事项[22] 乙炔的包装法通常是溶解在溶剂及多孔物中,装入钢瓶内。储存于阴凉、通风的易燃气体专用库房。远离火种、热源。库温不宜超过30℃。应与氧化剂、酸类、卤素分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备。小心避火。
乙炔合成方法常见问题
-
1.棉子壳或玉米芯制糖醛后的残渣(糠醛渣)或废山芋渣用稀酸加压水解可制得乙酰丙酸。将糖醛渣加入10%稀盐酸中,其固化液为1:1.75,混合均匀后投入水解锅,以0.2MPa压力的蒸汽蒸煮8-10h。然后...
-
在干燥的情性气体下,用34.1克(0.22摩尔)溴代苯,5.2克(0.21克)原子镁及108毫升无水制得格氏试剂。将所得之苯基溴化镁保存在惰性气体下,搅拌并用冰浴冷却,缓缓加入(15~20分钟) 6....
-
丙烯甲酯生产方法有:丙烯腈水解法、丙烯直接氧化法和乙烯酮法。1.丙烯腈水解法 以丙烯腈为原料,在浓存在的情况下进行水解,水解后的丙烯酰胺盐再与甲醇进行反应得到丙烯酸甲酯。用丙烯腈水化法生产的丙烯酸甲酯...
纯乙炔为无色芳香气味的易燃气体。 而电石制的乙炔因混有硫化氢H2S、磷化氢PH3、砷化氢而有毒,并且带有特殊的臭味。熔点(118.656kPa)-80.8℃,沸点-84℃,相对密度0.6208(-82/4℃),折射率1.00051,折光率1.0005(0℃),闪点(开杯)-17.78℃,自燃点305℃。在空气中爆炸极限2.3%-72.3%(vol)。在液态和固态下或在气态和一定压力下有猛烈爆炸的危险,受热、震动、电火花等因素都可以引发爆炸,因此不能在加压液化后贮存或运输。微溶于水,溶于乙醇、苯、丙酮。在15℃和1.5MPa时,乙炔在丙酮中的溶解度为237g/L,溶液是稳定的。
因此,工业上是在装满石棉等多孔物质的钢瓶中,使多孔物质吸收丙酮后将乙炔压入,以便贮存和运输。为了与其它气体区别,乙炔钢瓶的颜色一般为乳白色,橡胶气管一般为黑色,乙炔管道的螺纹一般为左旋螺纹(螺母上有径向的间断沟)。
分子构型:直线型
杂化类型:sp杂化中心原子孤电子对数:0通常计量单位:m³;mm³;cm³;
密度:标准气压下1.17 kg/m³;在25摄氏度状况下,密度1.12 kg/m³。
包装方法:钢质气瓶
在乙炔气体分压等于101.325 kPa时,被一体积水所吸收的该气体体积(已折合成标准状况)
| 温度(℃) |
溶解度 |
温度(℃) |
溶解度 |
温度(℃) |
溶解度 |
| 0 |
1.73 |
25 |
0.93 |
70 |
0.25 |
| 5 |
1.49 |
30 |
0.84 |
80 |
0.15 |
| 10 |
1.31 |
40 |
0.65 |
90 |
0.05 |
| 15 |
1.15 |
50 |
0.50 |
||
| 20 |
1.03 |
60 |
0.37 |
1.性状:无色无味气体,工业品有使人不愉快的大蒜气味。[1]
2.熔点(℃):-81.8(119kPa)[2]
3.沸点(℃):-83.8(升华)[3]
4.相对密度(水=1):0.62(-82℃)[4]
5.相对蒸气密度(空气=1):0.91[5]
6.饱和蒸气压(kPa):4460(20℃)[6]
7.燃烧热(kJ/mol):-1298.4[7]
8.临界温度(℃):35.2[8]
9.临界压力(MPa):6.19[9]
10.辛醇/水分配系数:0.37[10]
11.闪点(℃):-17.7(CC)[11]
12.引燃温度(℃):305[12]
13.爆炸上限(%):82[13]
14.爆炸下限(%):2.5[14]
15.溶解性:微溶于水,溶于乙醇,丙酮、氯仿、苯,混溶于乙醚。[15]
16.van der Waals体积(cm³·mol⁻¹):23.100
17.van der Waals面积(cm²·mol⁻¹):3.480×10^9
18.Lennard-Jones参数(A):7.222
19.Lennard-Jones参数(K):128.7
20.临界密度(g·cm-3):2.32
21.临界体积(cm³·mol⁻¹):112.2
22.临界压缩因子:0.2687
23.偏心因子:0.187
24.气相标准燃烧热(焓)(kJ·mol⁻¹):-1301.10
25.气相标准生成热(焓)( kJ·mol⁻¹):228.2
26.气相标准熵(J·mol⁻¹·K⁻¹) :200.92
27.气相标准生成自由能( kJ·mol⁻¹):210.7
28.气相标准热熔(J·mol⁻¹·K⁻¹):43.99
1836年,英国著名化学家戴维·汉弗莱(Davy,HumPhry1778-1829)的堂弟,爱尔兰港口城市科克(Cork)皇家学院化学教授戴维·爱德蒙德(Davy,Edmund1785-1857)在加热木炭和碳酸钾以制取金属钾过程中,将残渣(碳化钾)投进水中,产生一种气体,发生爆炸,分析确定这一气体的化学组成是C、H(当时采用碳的原子量等于6计算),称它为“一种新的氢的二碳化物”。这是因为早在1825年他的同国化学家法拉第(Faraday,MIChael1791-1867)从加压的蒸馏鲸鱼油获得的气体(供当时欧洲人照明用)中也获得一种碳和氢的化合物,分析测定它的化学组成是C、H,命名它为“氢的二碳化物”。实际上法拉第发现的是苯,戴维·爱德蒙德发现的是乙炔。
乙炔基本信息
中文名称:乙炔(音quē)
英文名称:acetylene
中文别名:乙炔气;溶解乙炔
英文别名:ethenylene; Ethine; Ethyne; Narcylen; Welding Gas
CAS号:74-86-2
分子式:C2H2
结构式:H-C≡C-H(直线型)
结构简式:HC≡CH
相对分子质量:26.0373
乙炔电石法
由电石(碳化钙)与水作用制得。
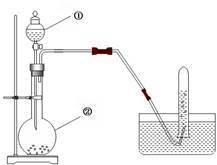
实验室中常用电石跟水反应制取乙炔。与水的反应是相当激烈的,可用分液漏斗控制加水量以调节出气速度。也可以用饱和食盐水。
原理:电石发生水解反应,生成乙炔。装置:烧瓶和分液漏斗(不能使用启普发生器)。烧瓶口要放棉花,以防止泡沫溢出。
试剂:电石(CaC₂)和水。
反应方程式:CaC₂ 2H-OH→Ca(OH)₂ CH≡CH↑
收集方法:排水集气法 或向下排空气集气法(不常用)
尾气处理:点燃
制备装置与氢气等气体类同。
乙炔天然气法
天然气制乙炔法
预热到600-650℃的原料天然气和氧进入多管式烧嘴板乙炔炉,在1500℃下,甲烷裂解制得8%左右的稀乙炔,再用N-甲基吡咯烷酮提浓制得99%的乙炔成品。
乙炔可用以照明、焊接及切断金属(氧炔焰),也是制造乙醛、醋酸、苯、合成橡胶、合成纤维等的基本原料。
乙炔燃烧时能产生高温,氧炔焰的温度可以达到3200℃左右,用于切割和焊接金属。供给适量空气,可以完全燃烧发出亮白光,在电灯未普及或没有电力的地方可以用做照明光源。乙炔化学性质活泼,能与许多试剂发生加成反应。在20世纪60年代前,乙炔是有机合成的最重要原料,现仍为重要原料之一。如与氯化氢、氢氰酸、乙酸加成,均可生成生产高聚物的原料。
乙炔在不同条件下,能发生不同的聚合作用,分别生成乙烯基乙炔或二乙烯基乙炔,前者与氯化氢加成可以得到制氯丁橡胶的原料2-氯-1,3-丁二烯。乙炔在400~500℃高温下,可以发生环状三聚合生成苯;以氰化镍Ni(CN)2为催化剂,在50℃和1.2~2MPa下,可以生成环辛四烯。
乙炔在高温下分解为碳和氢,由此可制备乙炔炭黑。一定条件下乙炔聚合生成苯,甲苯,二甲苯,,萘,蒽,苯乙烯,茚等芳烃。通过取代反应和加成反应,可生成一系列极有价值的产品。例如乙炔二聚生成乙烯基乙炔,进而与氯化氢进行加成反应得到氯丁二烯;乙炔直接水合制取乙醛;乙炔与氯化氢进行加成反应而制取氯乙烯;乙炔与乙酸反应制得乙酸乙烯;乙炔与氰化氢反应制取丙烯腈;乙炔与氨反应生成甲基吡啶和2-甲基-5-乙基吡啶;乙炔与甲苯反应生成二甲苯基乙烯,进一步催化剂裂化生成三种甲基苯乙烯的异构体:乙炔与一分子甲醛缩合为丙炔醇,与二分子甲醛缩合为丁炔二醇;乙炔与丙酮进行加成反应可制取甲基炔醇,进而反应生成异戊二烯;乙炔和一氧化碳及其他化合物(如水,醇,硫醇)等反应制取丙烯酸及其衍生物。
1、现场应急监测方法
(1)气体检测管法。
(2)气体速测管。
2、实验室监测方法
| 监测方法 |
类 别 |
来 源 |
|
| 气相色谱法 |
空气 |
《工作场所有害物质监测方法》 |
徐伯洪,闫慧芳主编 |
| 气相色谱法 |
空气 |
《空气中有害物质的测定方法》(第二版) |
杭士平编 |
| 乙炔亚铜比色法 |
空气 |
《化工企业空气中有害物质测定方法》 |
化学工业出版社 |
3、现场监测方法
(1)2M004乙炔气体传感器检测微量传感器。
(2)K204乙炔模块检测乙炔泄露。
CAS号:74-86-2
EINECS号:200-816-9
乙炔应急处置
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给予输氧。如呼吸停止,立即进行人工呼吸,就医。
呼吸系统防护:一般不需要特殊防护,但建议特殊情况下佩带合适的自吸过滤式防毒面具(氧气含量与空气中氧含量一致或接近时)。
眼睛防护:一般不需要特殊防护,高浓度接触时可戴化学安全防护眼镜。
身体防护:穿防静电工作服。
手防护:戴一般作业防护手套。
其他防护:工作现场严禁吸烟。避免长期反复接触。进入罐、限制性空间或其他高浓度区作业,必须有人监护。
泄漏应急处理:迅速撤离泄漏污染区人员至上风处,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿防静电工作服。尽可能切断泄漏源。合理通风,加速扩散。喷雾状水稀释、溶解。构筑围堤或挖坑以收容产生的大量废水。如有可能,将漏出气用排风机送至空旷地方或装设适当喷头烧掉。漏气容器要妥善处理,修复、检验后再用。
有害燃烧产物:一氧化碳、二氧化碳。
灭火方法:切断气源。若不能切断气源,则不允许熄灭泄漏处的火焰。喷水冷却容器,可能的话将容器从火场移至空旷处。
灭火剂:雾状水、泡沫、二氧化碳、干粉。
乙炔应急医疗
诊断要点:
(1)吸入一定浓度后有轻度头痛、头昏。
(2)吸入高浓度时先兴奋、多语、哭笑不安,继而头痛、眩晕、恶心、呕吐、步态不稳、嗜睡。
(3)严重者昏迷。
(4)乙炔急性毒性主要是因为高浓度时置换了空气中的氧,引起单纯性窒息作用,缺氧是主要致死原因。
预防措施:
停止吸入,症状迅速消失。实际上,乙炔中毒者的症状部分由于混入的磷化氢、硫化氢和其他气体所致。应注意有否混合气体中毒,尤其是磷化氢中毒的可能性,以便及时抢救。
乙炔毒理学资料
急性毒性:
纯乙炔属微毒类,具有弱麻醉和阻止细胞氧化的作用。高浓度时排挤空气中的氧,引起单纯性窒息作用。乙炔中常混有磷化氢、硫化氢等气体,故常伴有此类毒物的毒作用。人接触100 mg/m3能耐受30~60 min,20%引起明显缺氧,30%时共济失调,35%下5 min引起意识丧失,含10%乙炔的空气中5 h,有轻度中毒反应。
亚急性和慢性毒性:
动物长期吸入非致死性浓度该品,出现血红蛋白、网织细胞、淋巴细胞增加和中性粒细胞减少。尸检有支气管炎、肺炎、肺水肿、肝充血和脂肪浸润。
操作
密闭操作,全面通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员穿防静电工作服。远离火种、热源,工作场所严禁吸烟。使用防爆型的通风系统和设备。防止气体泄漏到工作场所空气中。避免与氧化剂、酸类、卤素接触。在传送过程中,钢瓶和容器必须接地和跨接,防止产生静电。搬运时轻装轻卸,防止钢瓶及附件破损。配备相应品种和数量的消防器材及泄漏应急处理设备。
储存
乙炔的包装法通常是溶解在溶剂及多孔物中,装入钢瓶内。储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。应与氧化剂、酸类、卤素分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备。
运输
采用钢瓶运输时必须戴好钢瓶上的安全帽。钢瓶一般平放,并应将瓶口朝同一方向,不可交叉;高度不得超过车辆的防护栏板,并用三角木垫卡牢,防止滚动。运输时运输车辆应配备相应品种和数量的消防器材。装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。严禁与氧化剂、酸类、卤素等混装、混运。夏季应早晚运输,防止日光曝晒。中途停留时应远离火种、热源。公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。铁路运输时要禁止溜放。
废弃处理
处置前应参阅国家和地方有关法规。建议用焚烧法处置和填埋。
1.本品具有麻醉作用,其麻醉性比单烯烃强得多。高浓度乙炔气爆炸危险性比毒性事故多。乙炔有阻止氧化的作用,使脑缺氧,引起昏迷麻醉,但对生理机能没有影响。吸入高浓度乙炔后,呈现酒醉样兴奋,能引起昏睡、紫绀、瞳孔发直、脉搏不齐等。苏醒后有对相关事故的发生经过丧失记忆能力等症状。停止吸入即迅速好转。发生中毒时应迅速脱离中毒现场,进行治疗。此外,应注意乙炔中常含有的磷化氢和砷化氢等杂质引起的中毒。
2.与空气形成爆炸性混合物。
3.性质很活泼,能起加成反应和聚合反应。
4.在氧化中燃烧可发生高温和强光。
5.稳定性[18] 稳定
6.禁配物[19] 强氧化剂、碱金属、碱土金属、重金属尤其是铜、重金属盐、卤素
7.聚合危害[20] 聚合
8.分解产物[21] 碳、氢
由于三键中的化学能,乙炔在压力超过100 kPa下会发生分解反应,此反应为放热反应,因此可引发剧烈的爆炸。液态或固态乙炔也会发生相同的分解反应,因此高压乙炔必须溶解在丙酮或二甲基甲醯胺中,并置于含有多孔性材质(Agamassan)的钢瓶中储存。
乙炔合成方法文献

 塞来昔布合成方法与杂质研究
塞来昔布合成方法与杂质研究
中图分类号: R9 密级:公开 UDC:615 学校代码: 10082 硕士学位论文 (同等学力人员) 塞来昔布合成方法与杂质研究 论 文 作 者: 崔志艳 指 导 教 师: 刘玉真 教授 副 指 导 教 师: 申请学位类别: 医学硕士 学 科 、 领 域: 药物化学 所 在 单 位: 化学与制药工程学院 答 辩 日 期: 年 月 日 Hebei University of Science and Technology Dissertation for the Master Degree Study on the Synthesis and Impurity of Celecoxib Classified Index:R9 Secrecy Rate:Publicized UDC:615 University Code:10082 Candidate: Cui Zhiyan S
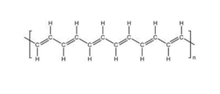
聚乙炔结构
聚乙炔包括单双键交替的共轭结构。由于双键不可扭转的性质,聚乙炔的每个结构单元都有顺式和反式两种结构。如果每个结构单元都呈顺式,则成为顺式聚乙炔,反之为反式聚乙炔。两者的电导率分别为10和10/欧·厘米。
通常乙炔瓶内的多孔性填料是采用质轻而多孔的活性炭、木屑、浮石以及硅藻土等合制而成的。将乙炔瓶逐支检查,并清洁气瓶上的污物和异物。检查瓶体是否有烧损、变形,涂层烧毁(漆皮鼓泡除外),瓶阀或易熔合金塞上易熔合金熔化及乙炔回火迹象。
检查乙炔瓶的检验周期是否过期。
检查乙炔瓶瓶身是否有裂纹或鼓包或凹陷变形或划伤及底座拼接焊缝开裂等问题。
检查乙炔瓶瓶身各处腐蚀情况,尤其是认真检查乙炔瓶底部及边缝腐蚀情况。
检查乙炔瓶阀及附件是否缺陷、损坏。
检查乙炔瓶颜色是否脱落变色;若气瓶颜色不对,则认真检查确定是否乙炔瓶。若新瓶则应抽成真空,补加丙酮。打开气瓶阀,用余压表测量气体余压时,检查气瓶的内芯、阀杆是否完好不打滑。
英文名称:Acetylene black
中文名称: 乙炔炭黑
又称:乙炔黑,简称ACET。
- 相关百科
- 相关知识
- 相关专栏
- 茼属植物
- 迎春花卉1
- 氯化反应
- 探火管
- Z41H低压明杆铸钢闸阀
- 气体质量流量计
- 天然气管道
- MilliporeElix纯水仪
- pod
- 化学化工专业实习
- millipore elix
- 聚乙烯双面胶防腐内带
- 溶解气体
- milli-qadvantage
- 天然气切割
- Millipore超纯水机
- 多逆变器太阳能光伏并网发电系统的组群控制方法
- 有源配电网设备利用率影响因子体系及其价值计算方法
- 原来这就是辨别冷热水管正确方法商家终于肯说实话了
- 新的基于NGA/PCA和SVM的特征提取方法
- 定征复合板材粘接层性质的非线性超声兰姆波方法
- 圆形隧道反向曲线隧道中心线两种偏移计算方法的比较
- 主要用固体工业废渣生产硫铝酸盐水泥熟料的方法
- 含有彩色浆料和渗透墨水形成的陶瓷砖及制作方法
- 保护装置BUCK开关电源的PCB优化设计方法
- 有软弱下卧层时确定天然地基上基础底面积的简便方法
- 以水利项目为例分析社会稳定风险评估方法与要点
- 医院手术部新风机组盘管冬季冻裂问题分析及防止方法
- 再谈VRV空调系统设计与施工中有关问题的解决方法
- 有关CAD技术在水利工程设计中的实际应用方法
- 柴油机高压喷油管用钢、高压喷油管及其制造方法
- 用于制冷系统稳定运行时制冷剂分布测试的新方法
