疏水性氨基酸简介
疏水性氨基酸 hydrophobic amino acid
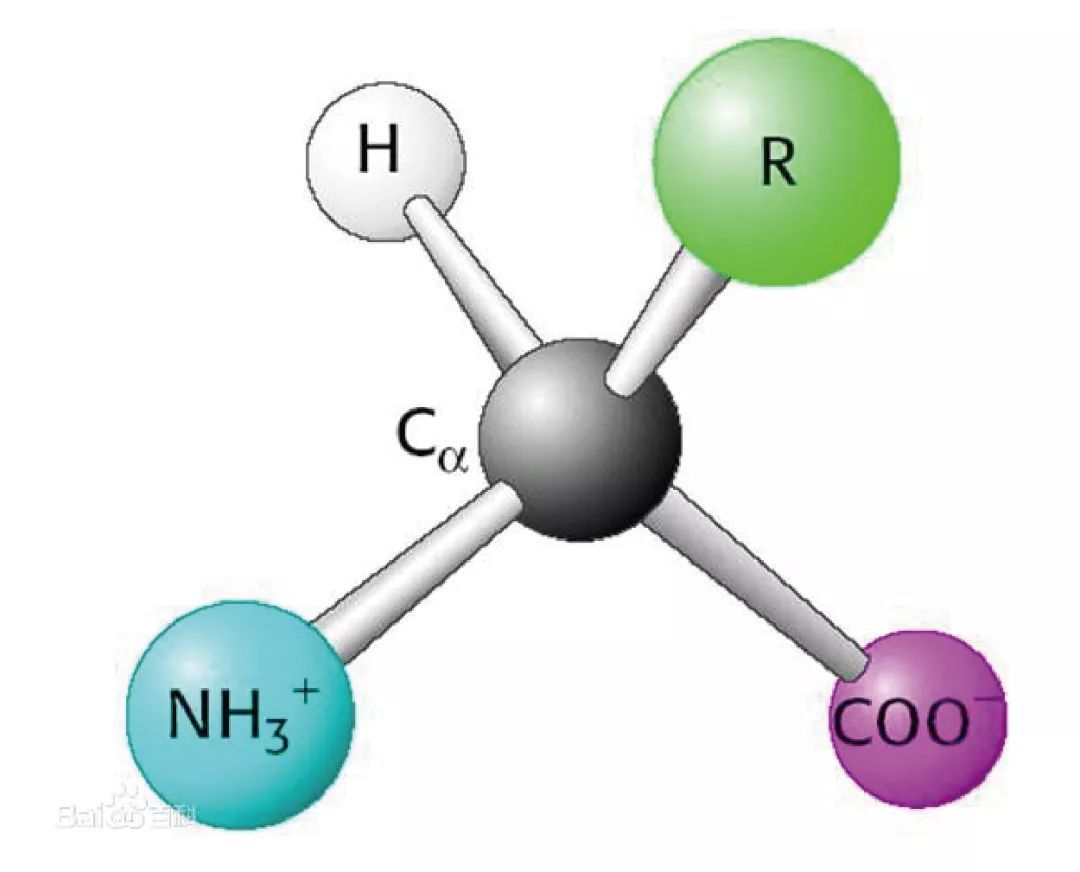
某溶质的疏水性(Hydrophobicity),是以其从水移于有机溶剂时的自由能的变化量来测定的,可通过在水和有机溶剂中的溶解度而测出。氨基酸侧链的疏水性,是从各氨基酸的疏水性减去甘氨酸疏水性之值来表示(C.Tanford)。疏水性氨基酸有色氨酸、苯丙氨酸、缬氨酸、亮氨酸、异亮氨酸、丙氨酸、脯氨酸和蛋氨酸(甲硫氨酸)。疏水性氨基酸在蛋白质内部,由于其疏水的相互作用,而在保持蛋白质的三级结构上起作用(参见疏水结合)。另外在酶和基质、抗体和抗原间的相互作用等各种非共价键的分子结合方面,具有重要作用,例如在抗体的与抗原结合的部位上有很多疏水性氨基酸,它参与与半抗原的结合。在维持生物膜的结构方面,疏水性氨基酸也具有作用,例如在红血球膜上存在的血型糖蛋白其膜内部分有许多疏水性氨基酸,形成一个疏水的区域。 2100433B
疏水性氨基酸造价信息
疏水性氨基酸简介常见问题
-
人体在食物中获得的八种氨基酸是:赖氨酸、色氨酸、苯丙氨酸、亮氨酸、异亮氨酸、苏氨酸、甲硫氨酸、缬氨酸。只是说在一段时间内要保持摄入氨基酸量的稳定,而且人体可以通过自身用 一种氨基酸合成另一种氨基酸。所...
-
没多少钱 跟市面上其他品牌的类似款差不多
-
价格各个地区不统一
疏水性氨基酸简介文献

 复合氨基酸粉替代豆粕水解液
复合氨基酸粉替代豆粕水解液
研制了可替代发酵培养基中豆粕水解液的一种复合氨基酸,优化了种子罐和发酵罐中复合氨基酸粉的添加配比。结果表明,复合氨基酸全部替代豆粕水解液,每吨理论酸可降低成本60元左右,产酸及转化率也得到提高,可以大幅度提高公司生产效益水平。

 纸层析法分离鉴定氨基酸.
纸层析法分离鉴定氨基酸.
纸层析法分离鉴定氨基酸.
1、氨基酸的甲醛滴定(formal titration)
氨基酸等电点原理
氨基酸虽然是一种两性电解质,即是酸性又是碱性,但它却不能直接用酸碱滴定来进行测量。这是因为氨基酸的酸碱滴定的等电点pH过高(12-13)或是过低(1-2)没有适合的指示剂可备选用。而向氨基酸中加入过量的甲醛,用氢氧化钠滴定时,由于甲醛可与氨基酸上的—N H3结合,形成—NH—CH2OH、—N(CH2—OH)2等羟甲基衍生物,而降低了氨基酸的碱性,相对增强了—N H3的解离,使滴定终点移到了pH9附近,在酚酞指示剂的变色区域内,能够用酚酞作为指示剂进行滴定。
以上出自《生物化学》(高等教育出版社 2006.5,王镜岩等主编)
氨基酸等电点流程
甲醛滴定法测定氨基酸含量
目的
初步掌握甲醛滴定法测定氨基酸含量的原理和操作要点
原理
水溶液中的氨基酸为兼性离子,因而不能直接用碱滴定氨基酸的羧基。甲醛可与氨基酸上的—N H3结合,形成—NH—CH2OH、—N(CH2—OH)2 等羟甲基衍生物,使N H3上的H 游离出来,这样就可以用碱滴定N H3放出H ,测出氨基氮,从而计算氨基酸的含量。
若样品中只含有单一的已知氨基酸,则可由此法滴定的结果算出氨基酸的含量。若样品中含有多种氨基酸(如蛋白质水解液),测不能由此法算出氨基酸的含量。
脯氨酸与甲醛作用后,生成的化合物不稳定,导致滴定后结果偏低;酪氨酸含酚基结构,导致滴定结果偏高。
材料、试剂与器具
(一)试剂
1、0.5%酚酞酒精溶液
称0.5g酚酞溶于100ml60%酒精中。
2、0.05%溴麝香草酚蓝溶液
取0.05溴麝行草酚蓝溶于100ml 20%乙醇溶液中。
3、1%甘氨酸溶液
取1g甘氨酸溶于100ml蒸馏水。
4、标准0.100mol/L 氢氧化钠溶液
5、中性甲本醛溶液
取甲醛溶液50ml,加0.5%酚酞指示剂约3ml,滴加0.1mol/LnaOH溶液,使溶液呈微粉红色,临用前中和。
(二)实验器具
1、锥形瓶 2、碱式滴定管
3、 移液管洗耳球 4、天平
5、容量瓶 6、试剂瓶
7、量筒 8、玻棒与烧杯
氨基酸等电点操作步骤
1、取3只100ml锥形瓶,按下表加入试剂
| 锥形瓶编号 试剂 |
样品1 |
样品2 |
空白 |
| 1%甘氨酸溶液或样品(ml) |
2.0 |
2.0 |
— |
| 蒸馏水(ml) |
5.0 |
5.0 |
7.0 |
| 中性甲醛溶液(ml) |
5.0 |
5.0 |
5.0 |
| 0.05%溴麝香草酚蓝溶液(滴) |
2 |
2 |
2 |
| 0.5%酚酞乙醇溶液(滴) |
4 |
4 |
4 |
2、混匀后用标准0.100mol/L氢氧化钠溶液滴定至紫色(pH8.7~9.0)
3、结果计算
每毫升氨基酸溶液中含氨基氮的毫克数为
式中:V1为滴定样品消耗氢氧化钠的体积(ml);
V2为滴空白消耗氢氧化钠的体积(ml);
1.4008 为1ml 0.1mol/L氢氧化溶液相当的氮量(mg)
氨基酸等电点注意事项
利用甲醛滴淀法可以用来测定蛋白质的水解程度。随着蛋白质水解度的增加,滴定值也增加,当蛋白质水解完成后,滴定值不再增加。
isoeletric point ,pI 定义:
2、氨基酸净电荷为零时的pH值。
3、氨基酸是两性电解质,在碱性溶液中表现出带负电荷,在酸性溶液中表现出带正电荷,在某一定pH溶液中,氨基酸所带的正电荷和负电荷相等时的pH,称为该氨基酸的等电点。

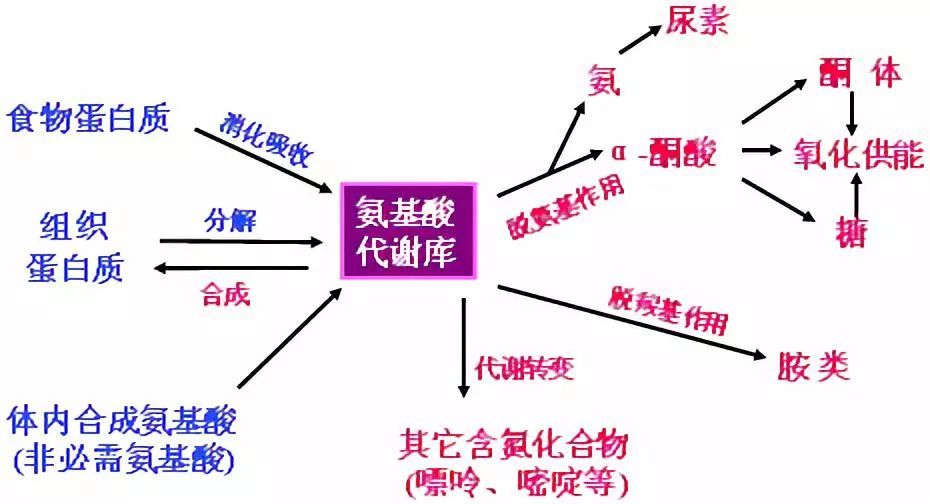
氨基酸是生命的基石,疾病与健康状况都与氨基酸有直接或间接的关联。氨基酸涉及代谢、肿瘤、免疫、心血管、神经系统、肾病、糖尿病、亚健康、老年病等各类疾病和人体生长发育、营养健康、肌肉骨骼生长、激素分泌、解毒功能的个个健康环节。
【什么叫营养代谢组学】
随着科技的发展和人类的进步,营养代谢组学逐渐进人了现代科学的研究范畴,发展成一门很重要的学科。代谢组学是继基因组学和蛋白质组学之后新近发展起来的一门学科,是系统生物学的重要组成部分。在营养支持方面代谢组学与系统生物学的其他技术一并用于研究营养表型(nutritional phenotype),后者被定义为基因组、蛋白质组、代谢组、功能和行为因素的集成系统。以前难以完成如此复杂的测定,而代谢组学技术的应用,可以测定许多营养代谢物与疾病及健康的关系。因此,代谢组学是唯一适合探索营养与代谢复杂关系的研究方法。
代谢组是指细胞在特定生理时期内所有的低分子量代谢产物总和,是全面认识一个生物系统不可或缺的一部分。如果说基因组学和蛋白质组学告诉我们可能发生的事件,那么代谢组学则可以告诉我们实际发生的事件,到目前为止人体内究竟有多少种代谢产物还很难说清楚,但包括脂肪、糖、氨基酸在内的各种底物以及代谢过程中生成的小分子化合物能够为了解机体健康状态提供重要信息。

代谢组学的研究才刚刚起步就已经迅速广泛地应用到了药物研发、分子生理病理学以及环境卫生等多个领域。相比于其他组学,代谢组学不仅能够给出庞大的数据库还可以提供一些功能信息。例如众所周知高胆固醇与心血管疾病风险相关,但高胆固醇水平只能提示机体可能存在某些健康问题,而代谢组学的研究可以对某一特定时期代谢产物的总和进行整体和动态分析,因此能够明确给出胆固醇增高的原因。因此这种方法对临床标本的检测最为实用。
【什么叫全谱氨基酸】
中文名:全谱氨基酸
英文名:full spectrum of amino acid
自然界的氨基酸种类很多,除常见的20种可组成蛋白质的氨基酸外,还有更多的氨基酸同样具有重要的生物学意义。人体中缺少某种氨基酸则影响人体健康,引发各种疾病,因此检测人体中氨基酸的缺少对治疗疾病有重要的意义。
全谱氨基酸是指氨基酸代谢组学中涉及的所有氨基酸。
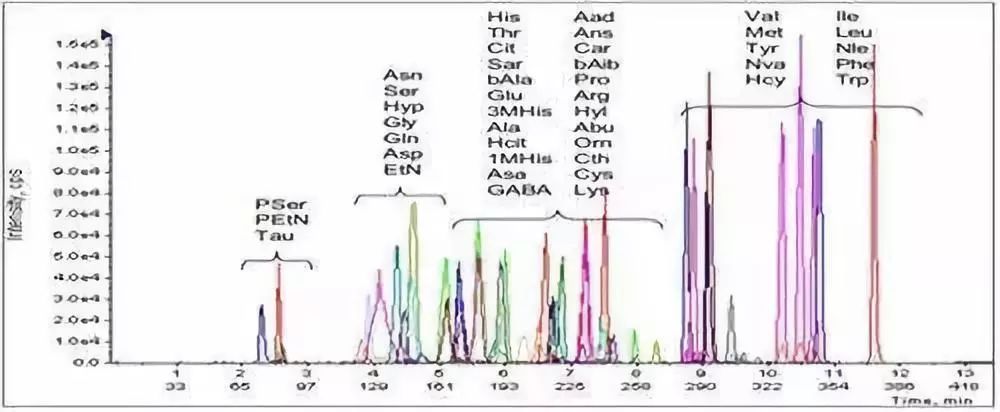
全谱氨基酸包括除组成蛋白的20种氨基酸外,还包括一些游离氨基酸和小肽,比如牛磺酸、γ-氨基丁酸(GABA)、肌酸、肌肽等。它们在某些方面对人体的重要作用并不比蛋白质氨基酸逊色,如:
牛磺酸与心脏的关系已成为全世界重点研究的课题之一。此外牛磺酸对肺、肝脏、胃肠等都有保护作用;肌氨酸、肌肽是一种天然抗氧化剂,具有延缓衰老、抗疲劳作用……

【人体43种全谱氨基酸分类】
A、8种必需氨基酸:
缬氨酸、异亮氨酸、亮氨酸、甲硫氨酸(蛋氨酸)、苯丙氨酸、色氨酸、苏氨酸、赖氨酸
B、6种半必需氨基酸(条件必需氨基酸):
组氨酸(儿童)、胱氨酸(含半胱氨酸)、酪氨酸、精氨酸、丝氨酸、甘氨酸。
C、6种非必需氨基酸:
丙氨酸、天门冬氨酸、谷氨酸、谷氨酰胺、脯氨酸、组氨酸
D、23种其他氨基酸(非蛋白氨基酸、游离氨基酸和小肽)
γ-氨基丁酸、牛磺酸、a-氨基已二酸、天门冬酰胺、瓜氨酸、鸟氨酸、胱硫醚、同型半胱氨酸、α-氨基正丁酸、鹅肌肽、b-丙氨酸、b-氨基异丁酸、肌肽、乙醇胺、δ-羟基赖氨酸、羟化脯氨酸、1-甲基组氨酸、3-甲基组氨酸、磷酸乙醇胺、磷酸酰丝氨酸、肌氨酸、精氨(基)琥珀酸、羟化瓜氨酸。

【全谱氨基酸代谢组学的意义】
目前,代谢组学是继基因组学、蛋白质组学、转录组学后出现的新兴“组学”,自1999年以来,每年发表的代谢组学研究的文章数量都在不断增加。代谢组学在新药的安全性评价、毒理学、生理学、重大疾病的早期诊断、个性化治疗、功能基因组学、中医药现代化、环境评价、营养学等科学领域中都有着极其广泛和重要的应用前景,是一门充满朝气的学科。

氨基酸是人类营养的基础,是最重要的营养组分,人类对氨基酸的研究比较广泛和系统,因此对氨基酸的研究又是营养组学中最为重要的一环。全谱氨基酸代谢组学打破以往只注重蛋白类氨基酸的传统,以全面的视角来检测和评估氨基酸代谢平衡。

全谱氨基酸在体内是一个平衡状态,全谱氨基酸的失衡是众多疾病的诱因或表现形式,涉及代谢、肿瘤、免疫、病毒、心脑血管、神经系统、肾病、糖尿病、亚健康、老年病等各类疾病和儿童生长发育、营养健康、肌肉骨骼生长、激素分泌、解毒功能等人体各种健康环节。目前氨基酸代谢障碍所引起的疾病已超过400多种。因此,全谱氨基酸代谢组学将在未来会对人类健康产生巨大的作用。
- 相关百科
- 相关知识
- 相关专栏
- 疏水性纤维
- 疏浚淤泥
- 疏花水柏枝
- 疣茎乌毛蕨
- 疲劳强度
- 疲劳强度试验机
- 病床电梯
- 痛·思-火灾警示录
- 登乘绳梯
- 登伯效应
- 登发
- 登封发祥磨料有限公司
- 登封市强力磨料磨具厂
- 登封市第二耐火材料有限公司
- 登封正立磨料磨具有限公司
- 白丁香无性系1号
- 永磁同步电机简介
- 乙酰丙酮测定水性内墙涂料中甲醛含量的不确定度评定
- 以色列ELI自清洗网式过滤器和浅层介质过滤器简介
- 应用工业废渣联合固化疏浚淤泥填筑路基施工技术分析
- 有关水利水电勘测设计技术标准体系情况的简介
- 改性聚磷酸铵在室内水性超薄型钢结构防火涂料中应用
- 工程技术分析论文地辐射采暖系统简介及常见问题
- 工程定额及造价资料电子查阅与简易预结算编制系统简介
- 国内深水环保疏浚方法和探索
- 基于C#地铁站安全疏散模糊综合评价系统开发与应用
- 广(州)深(圳)准高速铁路石龙—常坪段路基施工简介
- 含羟基叔氟微乳液合成及水性双组分聚氨酯清漆制备
- 基于GIS技术安徽省主要防洪工程信息系统简介
- 广东省东江—深圳供水改造工程施工图设计监理工作简介
- 乐星产电乐星产电(无锡)有限公司二期工程项目简介
- 国家玻璃质量监督检验中心安全玻璃CCC认证业务简介