三氧化二磷物理性质
摩尔质量:109.946g/mol
外观:无色单斜晶体或液体
密度:2.13g/cm3
熔点:23.8℃
沸点:175.3℃ (有资料说是173.1℃ )
pKa:9.2
三氧化二磷造价信息
三氧化二磷由白磷在有限的氧气中燃烧得到。该反应产率可达50%,产物中含少量白磷,可用汞弧灯照射将白磷转化为红磷,然后加热蒸出三氧化二磷而进行提纯(用CS2)。反应的副产物还有五氧化二磷和一氧化四磷。
P4+3O2→P4O6
用一氧化二氮(N2O)也可以制取P4O6:于823-873K,9.3kPa下使白磷和N2O反应生成P4O6。
把O2通入白磷的CCl4溶液,得浅黄色物,后者经真空干燥得白色P4O6.
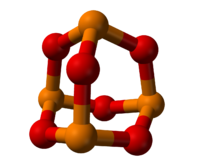
三氧化二磷结构
三氧化二磷(化学式:P4O6)是一种由氧和磷组成的化合物,为无色蜡状 有大蒜气味的极毒晶体,虽然它的正确名称应该是六氧化四磷,但以前一直以为分子结构是P2O3,因此三氧化二磷的名称一直沿用至今。
三氧化二磷为Td结构,其结构与金刚烷类似,可以看做是金刚烷中的四个叔碳被磷原子替代,而六个仲碳被氧原子替代。
三氧化二磷的偶极矩为0.
三氧化二磷物理性质常见问题
-
外观:棕黑色粉末熔点(℃):1567相对密度(g/cm3):4.718溶解性:不溶于水,溶于盐酸、。 其他性质:四氧化三锰在温度1443K以下时,四氧化三锰为扭曲的四方晶系尖晶石结构,而1443K以上...
-
现行教材《镁和铝的重要化合物》一节中有这样的叙述:“氧化镁是密度很小的白色粉末,它的熔点高达2800℃,是优良的耐火材料”;“氧化铝是一种白色难熔的物质……也是一种比较好的耐火材料”。学生会问:是氧化...
-
一 物理性质: 1. 纯硝酸是无色油状液体, 开盖时有烟雾, 挥发性酸[沸点低→易挥发→酸雾] 2. M.p. -42℃, b.p. 83℃. 密度: 1.5 g/cm3, 与水任意比互溶. ...
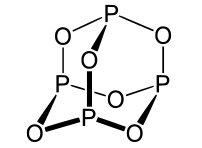
三氧化二磷简介
中文名:三氧化二磷
拼音:sānyǎnghuàèrlín
英文名称:diphosphorus trioxide 说明:P2O3或P4O6 又名亚磷酐。白色单斜晶体。有蒜臭。有毒!相对密度2.135(21℃)。在23.8℃时熔融为无色透明极易流动的液体。沸点为173℃.溶于乙醚、苯和二硫化碳。在直接日光即迅速氧化。在70℃时可引起燃烧。由磷在有限供给空气下燃烧而成。
三氧化二磷在气态或液态都是二聚分子P4O6,其中4个磷原子构成一个四面体,6个氧原子位于四面体每一棱的外侧,分别与两个磷原子形成P-O单键,每个磷原子与周围3个氧原子以O-P键连接形成一个四面体.其中3个氧原子是与另外3个四面体共用.P-O键长为165pm,键角POP为128度,OPO为99度.
可由五氧化二磷与磷在高温的条件下生成。3P2O5+4P=5P2O3
在冷水中能缓缓溶解形成亚磷酸,方程式为:P4O6+6H2O(冷)==4H3PO3
与热水发生猛烈作用则歧化为磷酸和膦或者单质磷
方程式为:P4O6+6H2O(热)==3H3PO4+PH3
或者:5P4O6+18H2O(热)==12H3PO4+8P
三氧化二磷化学性质
200-400°C时在密封管中减压加热三氧化二磷时,三氧化二磷分解为五氧化二磷和红磷:
2P4O6 → 3P2O4 + P(红磷)
三氧化二磷与过量冷水混合振荡反应时生成亚磷酸:
P4O6 + 6H2O → 4H3PO3
与热水的反应复杂且较为剧烈,生成红磷、磷化氢、亚磷酸和磷酸。
与氯、溴单质反应生成三氯氧磷和三溴氧磷。与碘反应很慢,生成红色的产物。加压条件下二者在四氯化碳中反应,析出橘红色的四碘化二磷: 5P4O6 + 8I2 → P2I4 +3P4O10
三氧化二磷与氯化氢(Hydrogen chloride)反应生成亚磷酸和三氯化磷:
P4O6 + 6HCl → 2H3PO3 + 2PCl3
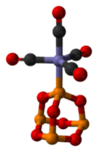
P4O6也可以作为配体(性质类似于亚磷酸根),取代四羰基镍或五羰基铁中的羰基,形成一系列的配合物。以P4O6·Fe(CO)4为例,该配合物有如图所示的结构,其中三氧化二磷是用一个磷原子与Fe配位(X射线单晶衍射数据)。
高于423K,S可以氧化P4O6:
P4O6+4S==P4O6S4
P4O6和B2H6反应生成H3BP4O6BH3:
P4O6+B2H6=H3BP4O6BH3
P4O6能取代羰基镍中的羰基,生成P4O6[Ni(CO)3]4、(P4O6)2Ni(CO)2、Ni(CO)(P4O6)3、Fe(CO)4(P4O6)。在最后一个化合物中,P4O6是一个磷原子和铁原子配位。
三氧化二磷物理性质文献

 焦炭的物理性质
焦炭的物理性质
焦炭的物理性质 焦炭物理性质包括焦炭筛分组成、焦炭散密度、焦炭真相对密度、 焦炭视相对密度、焦炭气 孔率、焦炭比热容、焦炭热导率、焦炭热应力、焦炭着火温度、焦炭热膨胀系数、焦炭收缩 率、焦炭电阻率和焦炭透气性等。 焦炭的物理性质与其常温机械强度和热强度及化学性质密切相关。焦炭的主要物理性质如下: 1. 真密度为 1.8-1.95g/cm3 ; 2. 视密度为 0.88-1.08g/ cm3 ; 3. 气孔率为 35-55%; 4. 散密度为 400-500kg/ m3 ; 5. 平均比热容为 0.808kj/ (kg?k)(100℃), 1.465kj/ ( kg?k)(1000℃); 6. 热导率为 2.64kj/ (m?h?k)(常温), 6.91kg/ (m?h?k)(900℃); 7. 着火温度(空气中)为 450- 650℃; 8. 干燥无灰基低热值为 30-32

 铜的物理性质综述
铜的物理性质综述
一、铜的物理性质包括导电性、导热性以及耐蚀性 1、铜的导电性 铜最重要的特性之一便是其具有极佳的导电性,其电导率为 58m/(Ω。mm 的平方 )。这 一特性使得铜大量应用于电子、 电气、电信和电子行业。 铜的这种高导电性与取原子结构有 关:当多个单独存在的铜原子结合成铜块时, 其价电子将不再局限于铜原子之中, 因而可以 在全部的固态铜中自由移动,其导电性仅次于银。铜的导电性国际标准为:一长 1m 重 1g 的铜在 20℃时的导电量公认为 100%。现在的铜炼技术已经可以生产出同品级铜的导电量比 这个国际标准高出 4%~5%。 2、铜的导热性 固体铜中喊有自由电子所产生的另一重要效应就是其拥有极高的导热性,其热导性为 386W/(m.k) ,导热性仅次于银。加之铜比金、银储量更丰富,价格更便宜,因此被制成电线 电缆、接插件端子、汇流 [排、引线框架等各种产品,广泛用于电子电气、电讯和电子行
化学成分包括:二氧化硅含量65.17%、三氧化二铝含量12.93%、氧化铁含量7.87%,同时还含有氧化钠、氧化锰、三氧化二磷、氧化钾、氧化钙和二氧化钛等多种物质。
用雾状水、干粉、抗溶性泡沫、二氧化碳、砂土灭火。用水保持火场中容器冷却。
储运须知
包装标志:易燃液体。包装方法:(Ⅲ)类。玻璃瓶外木箱,内衬不燃材料或铝桶、镀锌铁桶。储运条件:储存于阴凉、通风的仓间内。远离火种、热源。与卤代烃、硝酸盐和硝酸酯、甲烷二异氰酸酯、四氯化碳、三氧化二磷、三乙基铝、氧化剂和酸类隔离储运。搬运时轻装轻卸,保持包装完整。
泄漏处理
首先切断一切火源,戴好防毒面具与手套。用水冲洗,经稀释的污水放入废水系统。
接触机会
主要用作萃取乙炔和制造聚丙烯腈纤维的溶剂,亦用于有机合成、染料、制药、石油提炼和树脂等工业。在以上工作岗位可因接触DMF蒸汽而中毒。急性中毒发生原因多数由于生产故障,设备漏裂,或在检修设备时,未采取有效的防护措施,大量接触毒物所致,中毒常是吸入和皮肤吸收并存,且以皮肤吸收为主。
其他中毒情况少见,但有口服以及将该品灌肠作为治疗溃疡性结肠炎的药物而引起严重中毒的病例。
- 相关百科
- 相关知识
- 相关专栏
- 中国风景园林学会第三届第七次常务理事
- 引绰济辽工程远距离输水隧洞TBM施工三维数值模拟
- 中国造船工程学会被授予“第三届中国科协先进学会”
- 在听取四川省“三江”水电综合考察情况汇报时邹家华
- 在中国水利工程协会第三次全国会员代表大会上的讲话
- 引黄南干二级泵站进水压力钢管内壁防腐施工技术措施
- 云南绿水河二级电站4号水轮机增容技术改造效果分析
- 中国审计学会第七届常务理事会第二次会议
- 基于局部二进制模式的带钢表面缺陷初级检测方法
- 振冲灌注桩处理软土地基在谏壁二线船闸工程中的应用
- 云计算模型在船体复杂结构件装配和三维建模中的应用
- 中电三十八所无线测试塔工程复合土钉墙支护施工方案
- 招标文件(东太湖游泳池及驳岸二标段后审8.29)
- 云母/氟磷灰石生物玻璃陶瓷的体内外生物学性能
- 政府还贷二级公路收费站取消后治超工作的建议与对策
- 岳阳洞庭湖大桥50m跨连续箱形梁桥三向预应力施工